v=1903.9 m/s
La velocidad cuadrática media de una molécula sólo depende de la temperatura y su masa molecular. Podemos determinarla del valor de la energía cinética media de traslación de una molécula:
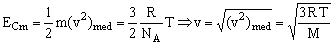
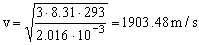
Podemos resolverlo también de la siguiente forma:
En condiciones normales, es decir, a 0ºC=273 K y 1 atm=760 mm de Hg, 1 mol de hidrógeno, que pesa 2.016 g ocupa 22.4 l. La densidad entonces será:
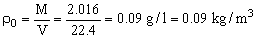
Las condiciones del problema son 70 cm de Hg=700 mm de Hg y 20ºC=293 K. Tendremos que determinar la densidad en estas condiciones:
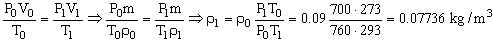
La presión de un gas en un recinto es debida a los choques de las moléculas contra las paredes del recinto. La presión viene dada por la expresión:
![]()
Si pasamos la presión al Sistema Internacional:
P1=700 mm de Hg=0.921 atm=93325.4 N/m2
De manera que tendremos:
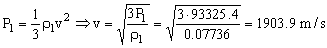
v=1903.9 m/s