a) Ec=7.719·10-21 J
b) Eescape=5.968·10-20 J
a) La energía cinética media será:
![]()
Y la energía cinética media de traslación de una molécula:
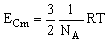
puesto que 1 mol tiene NA moléculas.
La temperatura vale:
T=100ºC=373 K
Sustituyendo en la ecuación de la energía:
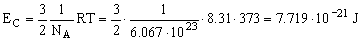
EC=7.719·10-21 J
b) El calor necesario para vaporizar 1 g de agua es de 539.55 cal. Vamos a ver lo que necesitamos para vaporizar una molécula. La masa de la molécula será:
![]()
Por tanto para vaporizar una molécula necesitamos una cantidad de calor:
Q=ml=2.989·10-23·535.55=1.612·10-20 cal
Esta energía estará dividida en dos partes, por un lado la energía cinética, y por otro la que utiliza para escapar. Tendremos entonces:
Q=EC+Eescape ⇒ Eescape=Q-EC
Necesitaremos tener todo en las mismas unidades. Pasamos las calorías a Julios:
Q=1.612·10-20 cal=6.740·10-20 J
Y sustituyendo:
Eescape=Q-EC=6.740·10-20-7.719·10-21=5.968·10-20 J
Eescape=5.968·10-20 J