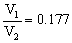a) T2=400 K; T1=800 K
b) 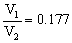
a) El trabajo en calorías será:
W=8360 J=2000 cal
Durante una expansión adiabática el calor intercambiado es nulo, luego aplicando el primer principio de la Termodinámica:
ΔQ=ΔU+W ⇒ 0=ΔU+W ⇒ -W=ΔU=ncVΔT=ncV(T2-T1)
El trabajo entonces será:
W=-ncV(T2-T1) ⇒ W=ncV(T1-T2)
![]()
Y teniendo en cuenta cómo se expresa el rendimiento en un ciclo de Carnot:
![]()
Tenemos un sistema de dos ecuaciones y dos incógnitas:
T1-T2=400
![]()
De la primera expresión:
T1-T2=400 Δ T1=400+T2
Y sustituyendo en la segunda:
![]()
T2=400 K
Y la otra temperatura:
T1=400+T2=400+400=800 K
T1=800 K
b) Como tenemos una expansión adiabática se debe verificar:
![]()
Por la ecuación de los gases perfectos:
![]()
![]()
Sustituyendo nos queda la expresión:
![]()
Tenemos que determinar el coeficiente de expansión adiabática. Sabemos que:
cP=cV+R=5+2=7 cal/molK
Por tanto:
![]()
Y volviendo a la expresión que habíamos obtenido:
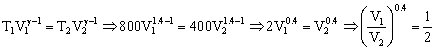
De donde obtenemos: