Problema de Calor y Primer Principio de la Termodinámica.
Problema de Calor y Primer Principio de la Termodinámica.
Problema de Calor y Primer Principio de la Termodinámica.
Problema de Calor y Primer Principio de la Termodinámica.
Cuestion de Calor y Primer Principio de la Termodinámica.
Cuestion de Calor y Primer Principio de la Termodinámica.
Problema de Calor y Primer Principio de la Termodinámica.

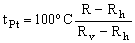 es la denominada temperatura del platino y Rh y Rv son, respectivamente, los valores de R en los puntos de hielo (0 oC) y de vapor de agua (100 oC). Las constantes δ y β son características del platino y están relacionadas con el comportamiento no lineal de la variación de R con t; si δ y β fueran nulas, la variación sería lineal y la temperatura del platino coincidiría con la temperatura Celsius. Considerando un termómetro para el que Rh=24.236 Ω y Rv=34.452 Ω, se pide: a) determinar las constantes δ y β teniendo en cuenta que en los puntos de ebullición normal del azufre (444.674 oC) y del oxígeno (-182.962 oC) la resistencia del termómetro es de 67.417 Ω y 5.927 Ω respectivamente, y que β=0 oC para t>>0 oC; b) calcular la temperatura correspondiente a una resistencia R=25.186 Ω.
es la denominada temperatura del platino y Rh y Rv son, respectivamente, los valores de R en los puntos de hielo (0 oC) y de vapor de agua (100 oC). Las constantes δ y β son características del platino y están relacionadas con el comportamiento no lineal de la variación de R con t; si δ y β fueran nulas, la variación sería lineal y la temperatura del platino coincidiría con la temperatura Celsius. Considerando un termómetro para el que Rh=24.236 Ω y Rv=34.452 Ω, se pide: a) determinar las constantes δ y β teniendo en cuenta que en los puntos de ebullición normal del azufre (444.674 oC) y del oxígeno (-182.962 oC) la resistencia del termómetro es de 67.417 Ω y 5.927 Ω respectivamente, y que β=0 oC para t>>0 oC; b) calcular la temperatura correspondiente a una resistencia R=25.186 Ω.